DETERMINACIÓN DEL
DIAGRAMA DE FASES
Existen esencialmente dos tipos
de métodos de estudio de los sistemas temperatura-composición. Aquellos en los
cuales se mantiene constante la temperatura y aquellos en los que se fija la
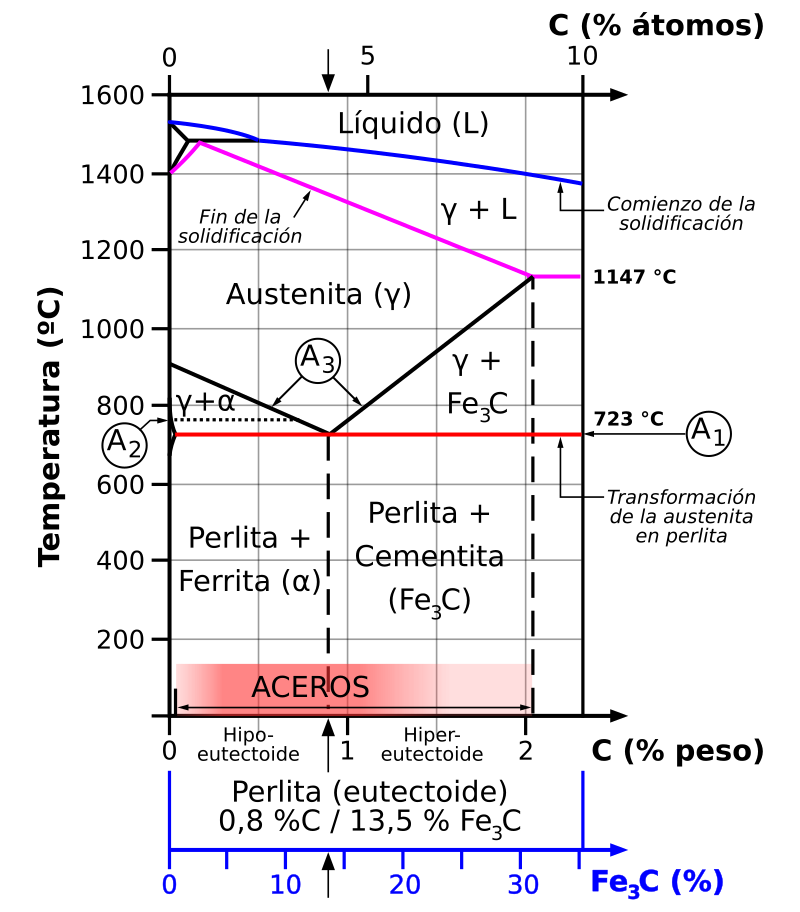
composición. Se puede estudiar el sistema a temperatura constante según T1 o T2
(Métodos isotérmicos), figura 1. Se puede también en un amplio margen de
temperaturas estudiar el comportamiento de unas muestras de composición fija
según X1 o X2 (Métodos de isocomposición).
MÉTODOS ISOTÉRMICOS
Medida de solubilidades. Permite el trazado de la curva de liquidus
mediante una separación de fases. Se separa la fase líquida de la fase sólida y
se determina la composición de la fase sólida a esa temperatura mediante medios
físicos o químicos.
Examen microscópico. Normalmente limitado al estudio de equilibrios
sólido/sólido y a temperatura ambiente, aunque existen equipos microscópicos
que permiten estudiar la variación de la microestructura con la temperatura ya que
incorporan algún sistema de calentamiento.
Este estudio permite determinar
la existencia de una o dos fases en el material y determinar los dominios de
existencia de las fases intermedias. Podemos asegurar que las microestructuras
observadas son de equilibrio ya que enfriamientos rápidos podrían llevar a
microestructuras metaestables.
Rayos X. Se procede igual que para estudios microscópicos, es
decir, las muestras de composiciones
diferentes se recuecen a una determinada temperatura, y después se templan. En el intervalo de una solución sólida monofásica, la red
cristalina es la misma pero el
parámetro de red cambia progresivamente con la composición. El límite de la solución sólida será aquel en el que
el parámetro de red permanece constante al
aparecer otra fase. A partir de ese punto, el parámetro de red no cambia ya que las dos fases tienen la misma
composición.

Medida de propiedades eléctricas. La más importante de todas es la
conductividad eléctrica. Se representa
en ordenadas la conductividad (inverso de la resistencia) a una temperatura constante y en abscisas la
composición en porcentaje en volumen obtenido
a partir de la densidad. En el primer caso los dos constituyentes están en estado puro y la gráfica presenta una
línea recta. Si los dos constituyentes forman una solución sólida, el gráfico da una curva continua con un mínimo.
En el caso de dos soluciones sólidas
terminales, se pueden distinguir los dominios monofásicos y el bifásico. Estas medidas no son siempre
fáciles ya que implican una preparación precisa
de las muestras y dependen mucho de los defectos mecánicos y de la presencia de impurezas.
MÉTODOS DE ISOCOMPOSICIÓN
Estos métodos se llaman
dinámicos, frente a los estáticos que se realizan a temperatura constante
(isotérmicos), se estudia la evolución de una propiedad física y requieren en
primer lugar alcanzar el estado de equilibrio. En los métodos de isocomposición
la temperatura varía constantemente con la medida y no se espera que se alcance
el equilibrio.
Análisis térmico. Es el método más importante dentro de este grupo.
Este tipo de métodos es, con diferencia, el más empleado. El principio es
bastante simple. Si la temperatura de un cuerpo que no sufre ningún cambio de
fase se determina en función del tiempo durante el enfriamiento, la curva
resultante no contendrá ningún salto. La existencia de un cambio de fase viene
acompañada de un intercambio de calor que da lugar un retraso en el
enfriamiento. En un componente puro cuando se alcanza la temperatura de
solidificación, la temperatura se mantendrá constante debido a que se genera el
calor latente de solidificación y a que al existir dos fases la temperatura
debe permanecer constante. Durante el tramo horizontal de la curva, van cambiando
las cantidades relativas de la fase sólida y líquida, hasta que se completa el paso
al estado sólido.

En realidad, vemos que en el
enfriamiento se sobrepasa ligeramente la temperatura de solidificación debido a
que se produce un subenfriamiento debido a los impedimentos para la nucleación
de la fase sólida. Cuando se produce por fin la nucleación y crecimiento la
solidificación es tan rápida que puede producirse un recalentamiento
prácticamente hasta la temperatura fusión al generarse el calor latente de
solidificación y producirse la transformación a la temperatura de fusión. El
final de la zona de temperatura constante no es abrupto. Normalmente existe un
redondeamiento de la curva debido a errores experimentales.
En el calentamiento la fusión
está precedida por un ligero sobre calentamiento y la zona de temperatura constante
cae ligeramente por encima de la temperatura de fusión de equilibrio. Estos
subenfriamientos y sobrecalentamientos son tanto menores cuanto menor sea la
velocidad de enfriamiento o calentamiento.

En los equilibrios bifásicos,
como la solidificación de una solución sólida, dan lugar a un cambio de
pendiente de la curva de enfriamiento, que marca el inicio de la
solidificación, que vuelve a cambiar cuando finaliza esta, produciéndose por tanto
en un intervalo de temperaturas. El subenfriamiento y la segregación pueden modificar
de forma importante la curva, figura Vuelve a aparecer un recalentamiento después
del subenfriamiento inicial que hace que la curva se aproxime al trazado ideal por
lo que la temperatura de liquidus se puede estimar extrapolando la zona de cambio
de pendiente de la curva. El retorno a la pendiente original de la curva de enfriamiento
indica la temperatura de solidus aunque su estimación es difícil debido al efecto
de la segregación. Los equilibrios bifásicos en estado sólido producen muy pocos
cambios en las curvas.
Los equilibrios invariantes, al ser isotérmicos
producen una curva semejante a la de solidificación de un componente puro. Las
curvas correspondientes a composiciones hipo e hipereutécticas son una mezcla
de las dos anteriores. En las reacciones peritécticas la zona isotérmica es
normalmente muy pequeña.
Basándose
en estos fenómenos el análisis térmico consiste en distintas técnicas que
estudian el comportamiento térmico de los materiales. Se trata de registrar
diversas propiedades de una muestra en función de la temperatura durante el
enfriamiento o calentamiento controlado (a velocidad constante) en una
atmósfera especifica. Los fenómenos exotérmicos (en enfriamiento) o
endotérmicos (en calentamiento) se ponen en evidencia y corresponden a líneas
que se cruzan en el diagrama (liquidus, solidus o invariantes). Para realizar
el análisis térmico el sistema ha de estar cerrado, es decir no se ha de
producir transferencia de materia del exterior al interior o a la inversa.
Al realizar el análisis térmico se puede
producir segregación, es decir, que a medida que se produce la solidificación
los cristales sólidos se vayan al fondo y el líquido que sobrenada tenga una
composición distinta, de tal forma que los datos recogidos por el termopar
varíen dependiendo de la posición del mismo. Para evitar esto es necesario
mantener el sistema agitado para homogeneizar la composición y para que los
cristales sólidos se distribuyan homogéneamente en el líquido. Otro problema
que puede producir errores es que el gradiente de temperatura dentro de la masa
no sea constante, sino que existan gradientes térmicos a lo largo de la masa.
Vamos
a comentar las que se utilizan con más frecuencia en la determinación de los
diagramas de equilibrio.
1.
Análisis térmico directo
Es el
más simple. Se trata de medir la variación de temperatura en intervalos
regulares de tiempo para distintas muestras de distintas composiciones. A
partir de esos datos se obtiene la curva de la figura 10 A. En ella se observa
que se pueden detectar cambios de pendiente que corresponden a cambios de
fases.
2.
Análisis térmico inverso
Se traza la curva de la variación de la
temperatura con el incremento del tiempo respecto a la temperatura. En este
caso se observa una mejor resolución de los puntos de modificación de la
pendiente de la curva, por lo que es un método más preciso.
3.
Análisis térmico derivado
Se traza la curva de variación de la
temperatura con la variación de la temperatura respecto al tiempo, donde se
muestran claramente los puntos de cambio de fases.
4. Análisis térmico
diferencial (ATD)
Se registra la diferencia de temperaturas deltaT
de una muestra con respecto a una muestra de referencia (material térmicamente
inerte en ese rango de temperaturas) en función del tiempo cuando se varia la
temperatura en una atmósfera controlada. Este método permite la detección de
cualquier tipo de transformación en todos los materiales. De esta manera se
pueden observar mejor los procesos térmicos ya que están mejor marcados que en
el análisis directo. En los equipos de ATD se utilizan termopares para medir la
temperatura de la muestra y de la referencia, y se representa la diferencia deltaT
entre ambas. deltaT está relacionada con el cambio de entalpía deltaH.
5.
Calorimetría diferencial de barrido (DSC)
Se determina en una atmósfera controlada la
variación del flujo de calor en una muestra en función de la temperatura. Tanto
en el enfriamiento como en el calentamiento cualquier transformación física o
química que ocurra en el material viene acompañada de un intercambio de calor.
Mediante la técnica de DSC se puede determinar la temperatura de la
transformación y se puede cuantificar la cantidad de calor que interviene. Es
una variación de la técnica anterior.
Dilatometría
Consiste en medir las variaciones de volumen
que acompañan a los cambios de fase en una aleación. Se estudia la evolución de
la longitud de una muestra durante el calentamiento o el enfriamiento. Se
registra la variación de longitud con la temperatura, pudiéndose observar que
se produce una variación del comportamiento cuando se pasa de un campo
monofásico a uno bifásico. En los equilibrios invariantes se produce un cambio
brusco de longitud. Las curvas de calentamiento y enfriamiento no se superponen
en la mayoría de los casos debido a los sobrecalentamientos y a los
subenfriamientos y se manifiesta un fenómeno de histéresis.
Podemos ver como a partir de los datos de
dilatometría de una muestra de composición determinada, se pueden determinar
los datos que permiten el trazado de las líneas del diagrama de equilibrio.
Difracción
de rayos X a temperatura variable
Se
puede obtener un diagrama de rayos X de la muestra mientras se eleva la
temperatura regularmente. Tiene el inconveniente de que hay que alcanzar el
equilibrio entre las dos fases durante el calentamiento para que los datos
obtenidos sean fiables.
Medidas
de conductividad eléctrica
Sirven para determinar la curva de solidus de
las soluciones sólidas ya que cuando comienza la fusión la resistencia
eléctrica de los metales aumenta fuertemente.
Método de temple
Se utiliza para observar el estado de equilibrio
obtenido a temperaturas elevadas. Se trata de utilizar una serie de muestras de
la misma composición a las que se las calienta a una temperatura determinada y
después de intervalos determinados de tiempo se sacan del horno y se templan.
Se evalúa la cantidad de fase transformada por algún método como el análisis de
imagen.
Métodos de observación directa
Se pueden utilizar microscopios con platinas
calientes o frías en las cuales se observan directamente los cambios de fase
que se van produciendo a medida que se calienta o de enfría un sistema.